|
低骨量人群是骨质疏松症的高危人群。国家卫健委骨质疏松症的流行病学调查显示,我国低骨量人群庞大,50岁以上人群低骨量率达到46.4%[1]。骨质疏松症已成为我国50岁以上人群(尤其是中老年女性)的重要健康问题。
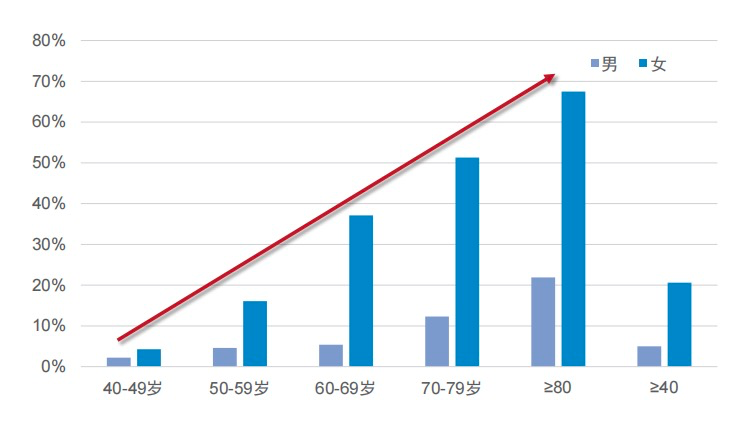
《中国骨质疏松白皮书》数据显示:2006年,我国骨质疏松症患者近7000万,骨量减少者超过2亿人[2];预计到2050年,我国骨质疏松症患者将会上升至1.2亿人[3]。医学界已将防治骨质疏松症放在了与治疗高血压、治疗高血脂同样重要的位置!
绝经后骨质疏松症(I型):一般发生在妇女绝经后5-10年内;老年性骨质疏松症(II型):一般于老年人70岁后发生。由任何影响骨代谢的疾病或药物及其他明确病因导致的骨质疏松。影响骨代谢的疾病:糖尿病、甲亢、血液系统疾病、其他代谢性骨病、肿瘤、肾脏病变等;影响骨代谢的药物:抗癫痫药物、糖皮质激素、其他免疫抑制剂等。骨是人体中钙、磷的最大储存库。人体骨组织不断地通过破骨和成骨作用与细胞外液进行钙磷交换,以维持血钙和血磷的稳定[4]。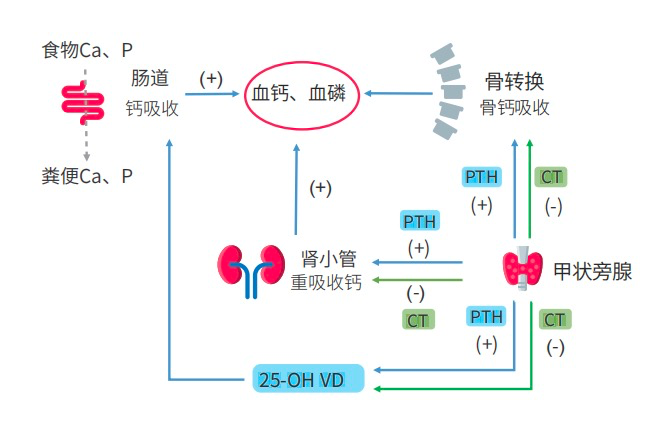
当血钙不够时,甲状旁腺素(PTH)分泌增加,作用于肾脏,促进肾小管重吸收钙,防止钙通过尿液流失;PTH也可以促进1,25(OH)2D的生成,促进肠道对钙、磷的吸收,提升血钙水平。
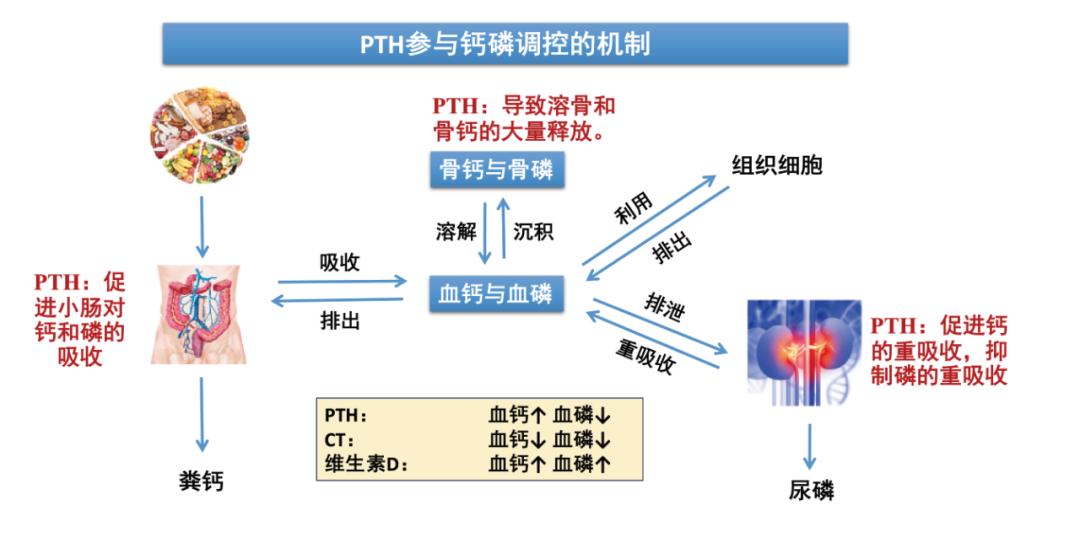
降钙素(CT)的作用与PTH相反,可降低血钙和血磷,作用的靶器官主要为骨和肾。主要是通过抑制破骨细胞的活动和促进成骨细胞的活动,以及增强肾脏对钙、磷的排泄而产生降低血钙和血磷的效应。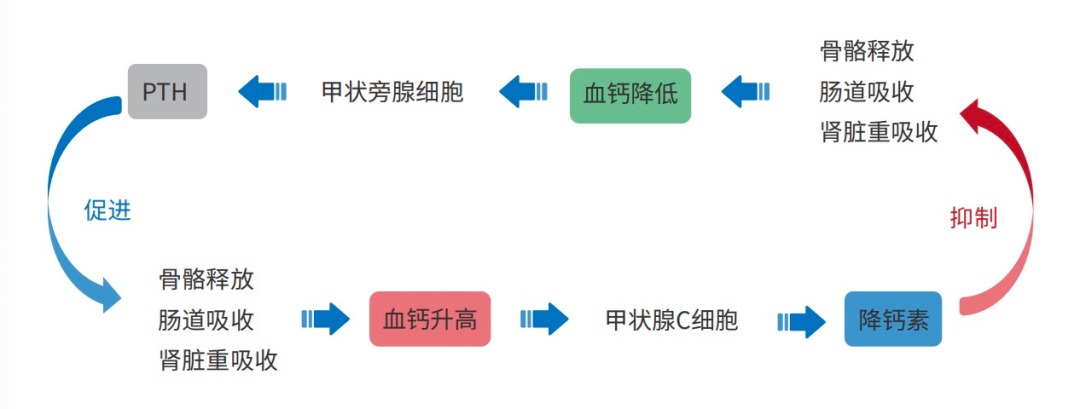
骨是人体最大的钙储存库,如果需要动用骨中的钙,就需要把钙从无机的状态中释放出来,这个过程也就是破骨细胞不断吸收旧骨和成骨细胞不断形成新骨的自我更新过程,称为骨转换(bone turnover)。
图源:Thomas M. Link, Judith E. Adams. Metabolic and Endocrine Skeletal Disease, Chapter 50.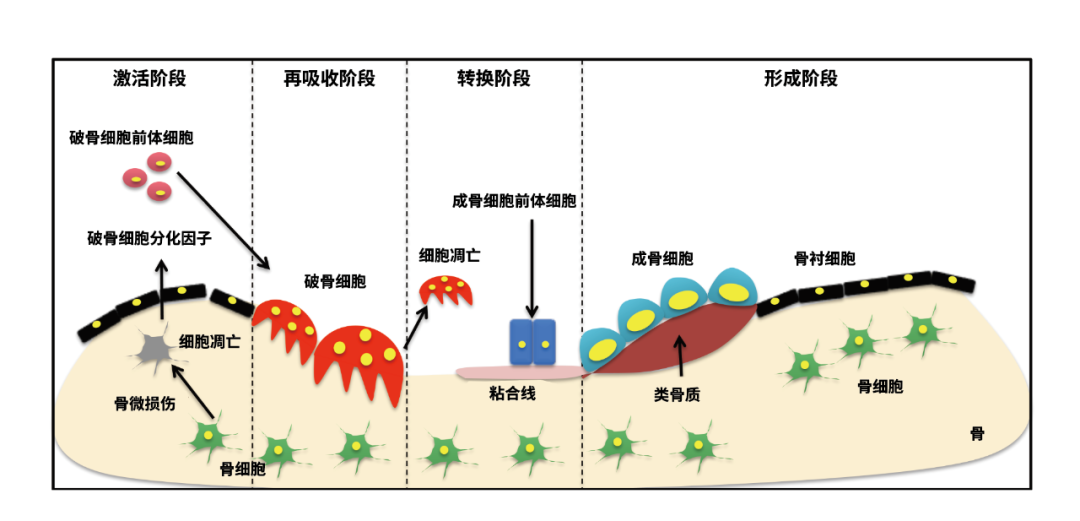
图源:Neha S. Dole, Genetic Determinants of Skeletal Diseases: Role of microRNAs, 2015骨代谢过程中产生的多种代谢产物储存于骨骼、血液、尿液或其他体液中,这些标志物统称为骨代谢标志物[5]。骨代谢标志物可及时反映骨转换状态,灵敏度高、特异性强,用于骨质疏松的诊断分型、骨折风险预测、抗骨质疏松治疗疗效评价,以及代谢性骨病的诊断与鉴别诊断。
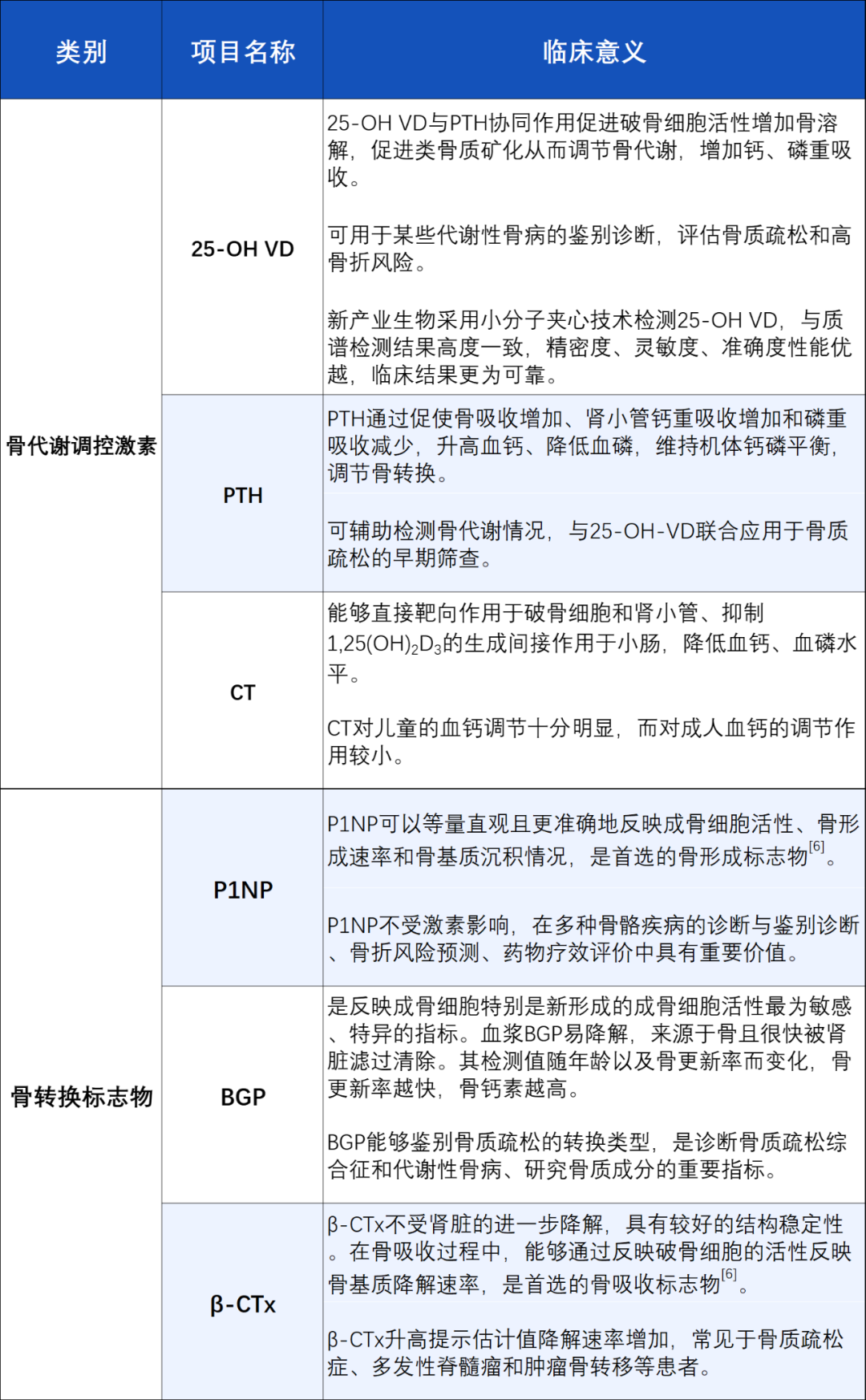
注:25-OH VD:25-羟基维生素D;PTH:甲状旁腺素;CT:降钙素;P1NP:I型前胶原氨基酸延长肽;BGP:骨钙素;β-CTx:β-胶原特殊序列骨转换标志物(bone turnover markers, BTMs)是在骨转换过程中产生的代谢产物或酶类,分为骨形成标志物和骨吸收标志物。检测骨转换标志物浓度对于多种骨骼疾病的诊断与鉴别诊断、骨折风险预测、药物疗效评价等具有重要价值。在疾病的诊断和治疗过程中,应至少选择一种骨形成标志物和一种骨吸收标志物。国际骨质疏松基金会(IOF)和国际临床化学和实验室医学联合会(IFCC)及多个指南共识均推荐,P1NP是首选的骨形成标志物,β-CTx是首选的骨吸收标志物[6-7]。
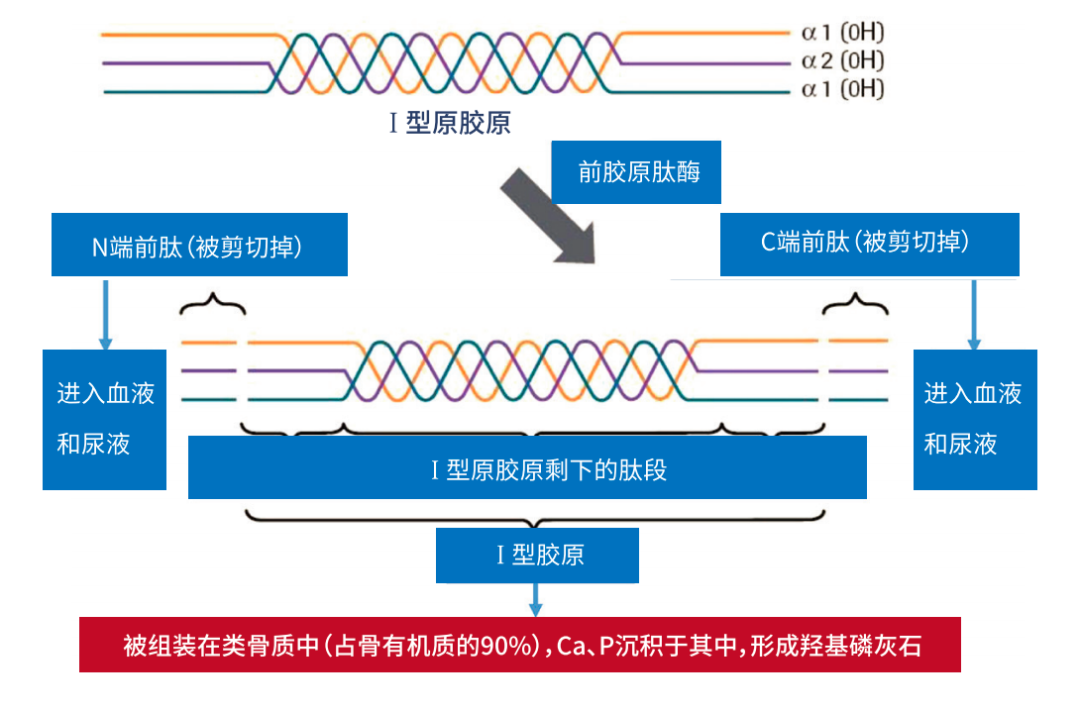
骨有机质中,90%以上为Ⅰ型胶原,是由Ⅰ型原胶原在蛋白酶作用下剪切掉氨基端前肽(P1NP)和羧基端前肽(P1CP)而形成。随后Ⅰ型胶原被组装在类骨质中,钙、磷、镁等矿物质沉积于其中,形成羟基磷灰石,而P1NP和P1CP则作为代谢产物进入血液和尿液中,能敏感地反映全身骨形成状态。
P1NP和P1CP与胶原分子存在1:1对应关系,均可反映胶原的合成及成骨细胞活性。但因P1CP代谢快,且易受激素水平影响,故P1NP更能准确反映成骨细胞活性。
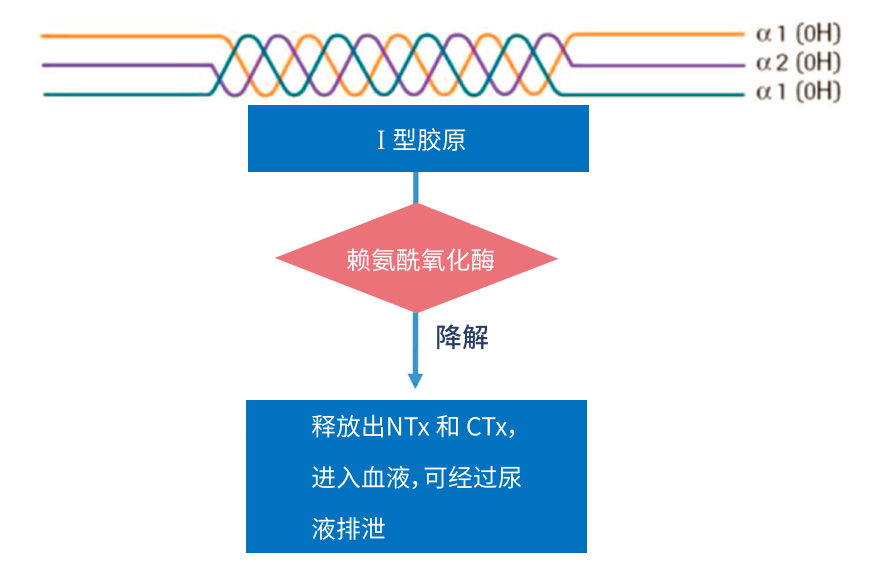
注:NTx-Ⅰ型胶原交联氨基端肽区(type Ⅰ collagen cross-linked N-telopeptide);CTx-Ⅰ型胶原交联羧基端肽区(type Ⅰ collagen cross-linked C-telopeptide) CTx是Ⅰ型胶原分解片段的一种,含有2条肽链,每条含有8个氨基酸,分子量约1700Da。CTx包含α-CTx和β-CTx两种,其中β-CTx是α-CTx的异构体,两者均含有Ⅰ型胶原分子间交联物的重要区段和近似交联物的残基,可保护其不受肾脏降解,稳定性较好。
血液及尿液中的CTx和NTx浓度能够特异性反映骨吸收水平,由于β-CTx作为骨吸收标志物的研究更多,为敏感而特异的骨吸收标志物。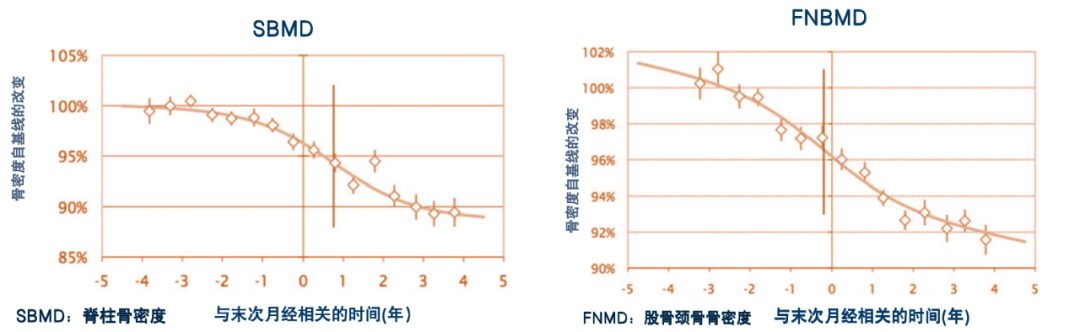
围绝经期和绝经早期女性的脊柱骨密度(SBMD)和股骨颈骨骨密度(FNBMD)变化图[8]
骨密度变化每年只有约1%左右,非常缓慢。而骨密度检测结果跟仪器、操作人员有很大关系,很难精确测定。无法反映围绝经期和绝经早期女性因雌激素快速变化而导致的骨量快速丢失。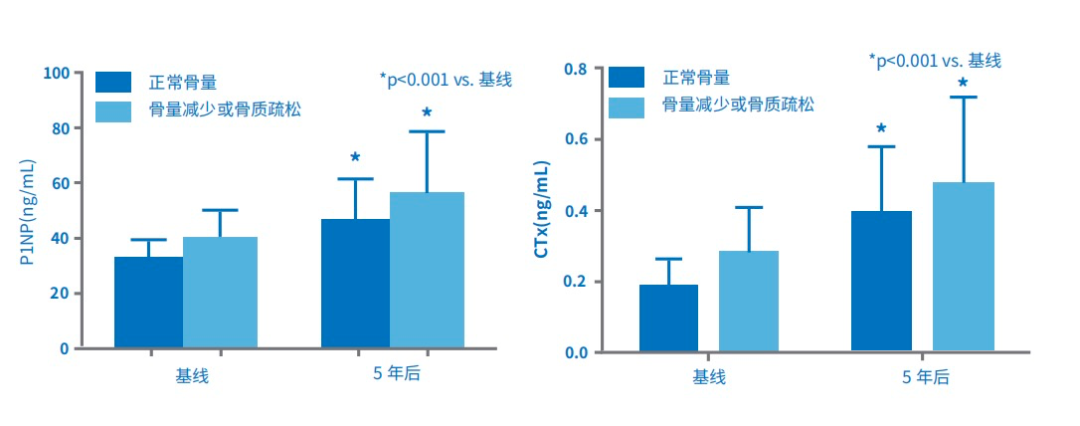
骨密度正常的女性的P1NP、CTx水平与骨量低或骨质疏松的女性比较图[9]
注:一项前瞻性研究共入组64名健康的绝经前妇女,平均年龄在44 - 57岁之间,随访5年。在基线和随访时评估患者的临床特征、生活方式、骨密度和BTMs (P1NP、CTx)。骨密度检测无法反映围绝经期和绝经早期女性的骨量快速丢失,而骨转换标志物可有效反映围绝经期骨量丢失。
IOF(国际骨质疏松基金会)建议,骨吸收标志物(如β-CTx)高于绝经前范围2个标准差,表明骨质疏松骨折风险大约增加2倍。β-CTx联合其他因素能更好评估骨折风险[10]。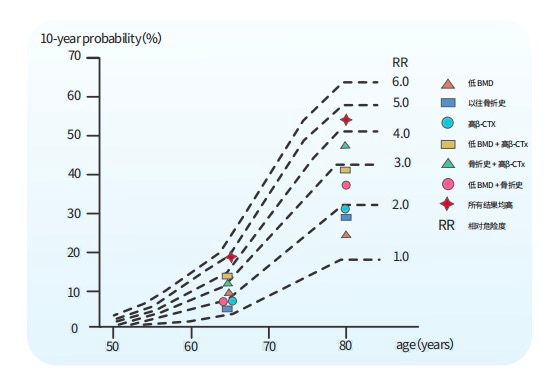
原发性骨质疏松症患者,除近期发生骨折,骨转换标志物通常在正常范围内或轻度升高;如果患者骨转换标志物超过正常上限的2倍,常提示患者可能存在继发性骨质疏松症等情况。
使用抗骨吸收治疗后,P1NP和CTx迅速下降;使用促骨形成药物后,P1NP和CTx迅速上升[12]。
使用抗吸收治疗(紫色)和促骨形成治疗(粉色)后,BTMs的变化幅度均值[12]
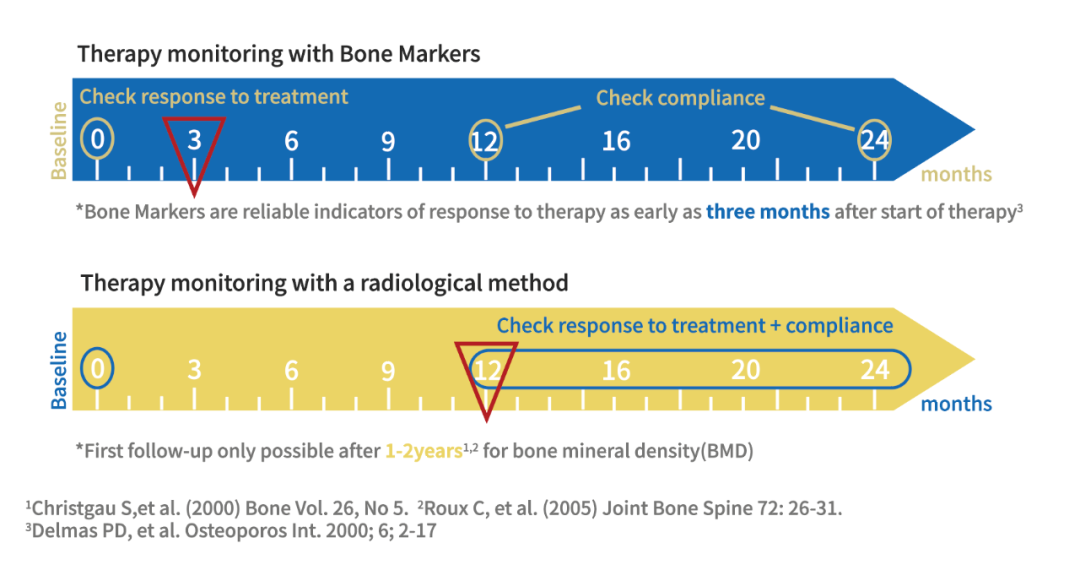
P1NP/β-CTx在治疗开始后三个月即可反馈治疗效果,BMD(骨密度)则要1-2年以后。P1NP和β-CTx可以应用于肿瘤患者骨转移的辅助诊断,尤其适用于肺癌、乳腺癌、前列腺癌患者。
图源:Anticancer research, 2004

图源:the official journal of the American Society for Bone and Mineral Research, 2005

图源:BMC Cancer, 2020 新产业基于先进的化学发光平台,提供了P1NP、β-CTx、BGP、PTH、CT、25-OH VD在内的骨代谢检测完整菜单,其中25-OH VD是国内首家实现小分子夹心法检测的商业化试剂,与质谱检测的一致性很好。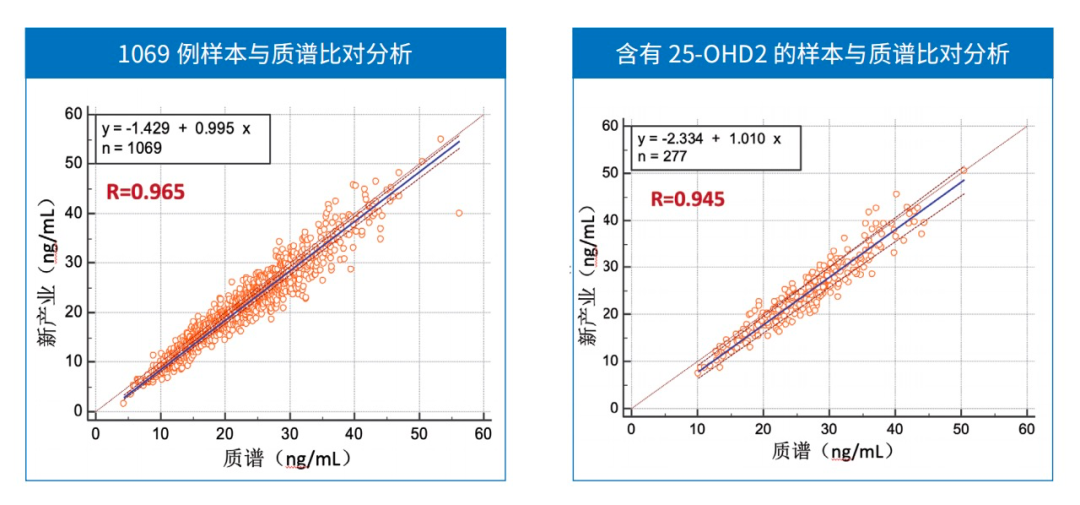
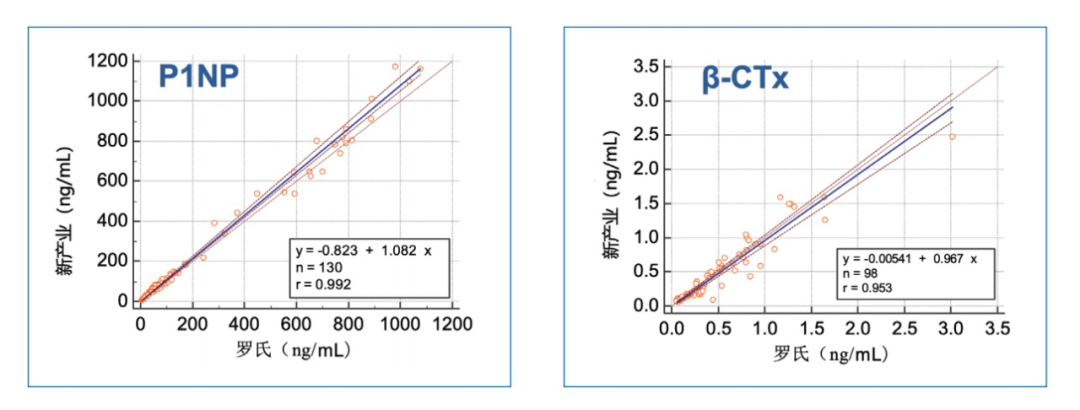
新产业生物骨代谢六项可为患者提供骨质疏松症的骨折风险评估、鉴别诊断及长期疗效监测,有效助力骨质疏松症的全过程管理。

2. 骨转换标志物可用于骨折风险预测、骨质疏松症的鉴别诊断及疗效监测
[1]Wang L, Yu W, Yin X, et al. JAMA network open, 2021, 4(8): e2121106-e2121106. [2]中国健康促进基金会骨质疏松防治中国白皮书编委会. 中华健康管理学杂志, 2009, 3: 148-154. [3]Zeng Q, Li N, Wang Q, et al. J Bone Miner Res, 2019, 34:1789-1797. [4]International Osteoporosis Foundation. IOF One-minute osteoporosis risk test, 2017. [5]Vilaca T, Gossiel F, Eastell R. J Clin Densitom, 2017, 20: 346-352. [6]Vasikaran S., Eastell R., Bruyère O. et al. Osteoporos Int, 2011, 22(2): 391-420. [7]中华医学会骨质疏松和骨矿盐疾病分会. 中华内分泌代谢杂志, 2021, 37(10) : 863-874. [8]Recker RR. Ann Ny Acad Sci, 2011, 1240: E26-30. [9]Gutierrez-Buey G et al. Clin Endocrinol (Oxf), 2019, 91(3): 391-399. [10]Johnell. Osteoporos Int, 2002, 13: 527-39. [11]中国健康促进基金会基层医疗机构骨质疏松症诊断与治疗专家共识委员会. 中国骨质疏松杂志, 2021, 27(7): 937-944. [12]Leder et al. J Clin Endocrinol Metab, 2014, 99(5): 1694-1700.
|