|
5月14日,国家卫生健康委发布了新型冠状病毒肺炎防控方案(第八版),同时作为附件发布了新冠病毒样本采集和检测技术指南。 
各省、自治区、直辖市及新疆生产建设兵团应对新型冠状病毒肺炎疫情联防联控机制(领导小组、指挥部),中国疾控中心:为进一步指导各地做好新型冠状病毒肺炎防控工作,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组制定了新型冠状病毒肺炎防控方案(第八版)。现印发给你们,请认真组织实施。各地在执行过程中如有相关建议,请及时反馈机制综合组。
《新冠病毒样本采集和检测技术指南》
为指导各级疾控部门和其他相关机构规范开展新冠肺炎病例标本采集与实验室检测工作,保证检测质量,提高检测效率,特制定本指南。
新冠肺炎病例、可疑感染人员和其他需要进行检测的人员,以及可能被污染的环境或物品等。从事标本采集的技术人员应当经过生物安全、监测技术培训并合格,熟悉标本采集方法,熟练掌握标本采集操作流程。应严格按照操作流程进行采样,按要求做好标本信息记录,确保标本质量符合要求、标本及相关信息可追溯。1.住院病例的标本由所在医院的医护人员采集,密切接触者标本由当地指定的疾控机构、医疗机构负责采集。采集标本时,要根据不同采集对象设置不同的采样区域,发热患者前往发热门诊就诊、采样,未设置发热门诊的机构应设置发热患者专用采样区域,将发热患者与其他检测人群分区采样,避免交叉感染。2.无症状感染者、入境人员、密切接触者在隔离观察期间应采集鼻咽拭子进行核酸检测,解除隔离时应同时采集 2 份鼻咽拭子样本,分别使用不同核酸检测试剂检测,2 次检测原则上由不同检测机构开展。3.根据临床及实验室检测工作的需要,可在住院、隔离期间多次采样,可同时采集呼吸道、血液、便等多种标本。采样人员应严格遵循采样规范采集标本,保障所采集标本质量符合要求,同时应详细记录受检者信息,可利用条形码扫描等信息化手段采集相关信息。4.人群筛查应根据核酸提取、检测所用试剂的要求确定采样管,可选择含病毒灭活剂(胍盐或表面活性剂等)的采样管。用于病毒分离的标本应放置于不含有病毒灭活剂的采样管。5.物品和环境监测应根据监测目的和防控需求,确定采样物品、位置与数量,采样时应严格遵循采样规范。每个病例必须采集急性期呼吸道标本(包括上呼吸道标本或下呼吸道标本),重症病例优先采集下呼吸道标本;根据临床需要可留取便标本、全血标本、血清标本和尿标本。物品和环境标本根据监测需求采集。2.下呼吸道标本:深咳痰液、肺泡灌洗液、支气管灌洗液、呼吸道吸取物等。3.便标本/肛拭子:留取粪便标本约10克(花生大小),如果不便于留取便标本,可采集肛拭子。4.血液标本:抗凝血,采集量5ml,建议使用含有EDTA 抗凝剂的真空釆血管采集血液。5.血清标本:尽量采集急性期、恢复期双份血清。第一份血清应当尽早(最好在发病后7天内)采集,第二份血清应当在发病后第3~4周采集。采集量5ml,建议使用无抗凝剂的真空采血管。血清标本主要用于抗体的测定,不进行核酸检测。7.物体表面标本:包括进口冷链食品或进口货物的内外包装表面,以及运输储藏工具等可能被污染的部位进行涂抹采集的标本。8.污水标本:根据海运口岸大型进口冷冻物品加工处理场所排水系统分布情况,重点选取污水排水口、内部管网汇集处、污水流向的下游或与市政管网的连接处等2~3处点位进行采样。1.鼻咽拭子:采样人员一手轻扶被采集人员的头部,一手执拭子,拭子贴鼻孔进入,沿下鼻道的底部向后缓缓深入,由于鼻道呈弧形,不可用力过猛,以免发生外伤出血。待拭子顶端到达鼻咽腔后壁时,轻轻旋转一周(如遇反射性咳嗽,应停留片刻),然后缓缓取出拭子,将拭子头浸入含2~3ml 病毒保存液(也可使用等渗盐溶液、组织培养液或磷酸盐缓冲液)的管中,尾部弃去,旋紧管盖。2.咽拭子:被采集人员先用生理盐水漱口,采样人员将拭子放入无菌生理盐水中湿润(禁止将拭子放入病毒保存液中,避免抗生素引起过敏),被采集人员头部微仰,嘴张大,并发“啊”音,露出两侧扁桃体,将拭子越过舌根,在被采集者两侧扁桃体稍微用力来回擦拭至少3次,然后再在咽后壁上下擦拭至少3次,将拭子头浸入含2~3ml病毒保存液(也可使用等渗盐溶液、组织培养液或磷酸盐缓冲液)的管中,尾部弃去,旋紧管盖。咽拭子也可与鼻咽拭子放置于同一管中。3.鼻咽抽取物或呼吸道抽取物:用与负压泵相连的收集器从鼻咽部抽取粘液或从气管抽取呼吸道分泌物。将收集器头部插入鼻腔或气管,接通负压,旋转收集器头部并缓慢退出,收集抽取的粘液,并用3ml采样液冲洗收集器1次(亦可用小儿导尿管接在50ml注射器上来替代收集器)。4.深咳痰液:要求病人深咳后,将咳出的痰液收集于含3ml采样液的采样管中。如果痰液未收集于采样液中,可在检测前,加入2~3ml采样液,或加入痰液等体积的痰液消化液。痰液消化液储存液配方见表1。使用时将储存液用去离子水稀释至50ml,与痰液等体积混合使用,或者参照试剂说明进行使用,也可采用痰液等体积的含1g/L蛋白酶K的磷酸盐缓冲液将痰液化。5.支气管灌洗液:将收集器头部从鼻孔或气管插口处插入气管(约30cm深处),注入5ml生理盐水,接通负压,旋转收集器头部并缓慢退出,收集抽取的粘液,并用采样液冲洗收集器1次,也可用小儿导尿管接在50ml注射器上来替代收集。6.肺泡灌洗液:局部麻醉后将纤维支气管镜通过口或鼻经过咽部插入右肺中叶或左肺舌段的支气管,将其顶端契入支气管分支开口,经气管活检孔缓缓加入灭菌生理盐水,每次30~50ml,总量100~250ml,不应超过300ml。7.粪便标本:取1ml标本处理液,挑取黄豆粒大小的便标本加至管中,轻轻吹吸3~5次,室温静置10分钟,以8000rpm离心5分钟,吸取上清液进行检测。粪便标本处理液可自行配制,配方见表2。也可使用HANK’S液或其它等渗盐溶液、组织培养液或磷酸盐缓冲液溶解便标本制备便悬液。如患者出现腹泻症状,则留取粪便标本3~5ml,轻轻吹打混匀后,以8000rpm离心5分钟,吸取上清液备用。8.肛拭子:用消毒棉拭子轻轻插入肛门3~5cm,再轻轻旋转拔出,立即放入含有3~5ml病毒保存液的15ml外螺旋盖采样管中,弃去尾部,旋紧管盖。9.血液标本:建议使用含有EDTA抗凝剂的真空采血管采集血液标本5ml,根据所选用核酸提取试剂的类型确定以全血或血浆进行核酸提取。如需分离血浆,将全血 1500~ 2000rpm离心10分钟,收集上清液于无菌螺口塑料管中。10.血清标本:用真空负压采血管采集血液标本5ml,室温静置30分钟,1500~2000rpm离心10分钟,收集血清于无菌螺口塑料管中。11.物体表面标本:参考《农贸(集贸)市场新型冠状病毒环境监测技术规范》(WS/T776—2021)推荐的方法,采样拭子充分浸润病毒保存液后在表面重复涂抹,将拭子放回采样管浸润,取出后再次涂抹采样,重复3次以上。对表面较大的物体进行多点分布式采样。12.污水标本:参考《农贸(集贸)市场新型冠状病毒环境监测技术规范》(WS/T776—2021)推荐的方法,采集污水的拭子样本时,用拭子浸入吸附污水,将拭子放回采样管浸润,取出后再次浸入污水,重复3次以上,对每个污水采样位置应进行多点分布式采样。采集污水的水体样本时,用聚乙烯塑料瓶收集1L~1.5L污水,大于1.5L体积的污水采集,可以使用聚乙烯塑料桶或现场水样专用富集设备。污水水体样本采集前,先充分混合均匀后取样;如果污水难以充分混合,出现分层现象时,可按各层水量的比例分层取样。1.所有标本应当放在大小适合的带螺旋盖内有垫圈、耐冷冻的样本采集管里,拧紧。容器外注明样本编号、种类、姓名及采样日期。2.将密闭后的标本装入密封袋,每袋限一份标本。样本包装要求要符合《危险品航空安全运输技术细则》相应的标准。3.涉及外部标本运输的,应根据标本类型,按照A类或B类感染性物质进行三层包装。用于病毒分离和核酸检测的标本应当尽快进行检测,可在24小时内检测的标本可置于4℃保存;24小时内无法检测的标本则应置于-70℃或以下保存(如无-70℃保存条件,则于-20℃冰箱暂存)。血清标本可在4℃存放3天,-20℃以下可长期保存。应当设立专库或专柜单独保存标本。标本采集后应当尽快送往实验室,标本采集后室温(25℃)放置不宜超过4小时。如果需要长途运输,建议采用干冰等制冷方式进行保藏。标本运送期间应当避免反复冻融。各省(自治区、直辖市)发现的本土疫情中的首发或早期病例、与早期病例有流行病学关联的关键病例、感染来源不明的本土病例、境外输入病例、入境物品及相关环境阳性标本等所有原始标本应平行采集至少2份,一份送各省级疾控机构进行检测,另一份上送中国疾控中心进行检测、复核,同时附样本送检单(见附件10-1)。各省分离到的新的代表性毒株,应及时送中国疾控中心复核、保藏。新冠病毒毒株或其它潜在感染性生物材料的运输包装分类属于A类,对应的联合国编号为UN2814,包装符合国际民航组织文件Doc9284《危险品航空安全运输技术细则》的PI620分类包装要求;环境样本属于B类,对应的联合国编号为UN3373,包装符合国际民航组织文件Doc9284《危险品航空安全运输技术细则》的PI650分类包装要求;通过其他交通工具运输的可参照以上标准包装。新冠病毒毒株或其它潜在感染性材料运输应按照《可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》(原卫生部令第45号)办理《准运证书》。在国际间运输的新冠病毒标本或毒株,应当规范包装,按照《出入境特殊物品卫生检疫管理规定》办理相关手续,并满足相关国家和国际相关要求。通过航空进行运送的标本抵达目的地机场后,由专业运输车辆运送至接收单位,通过陆路运输的标本由专业车辆进行运送,运送人员和接收人员应对标本进行双签收。新冠病毒标本及毒株应由专人管理,准确记录标本及毒株的来源、种类、数量,编号登记,采取有效措施确保毒株和样本的安全,严防发生误用、恶意使用、被盗、被抢、丢失、泄露等事件。
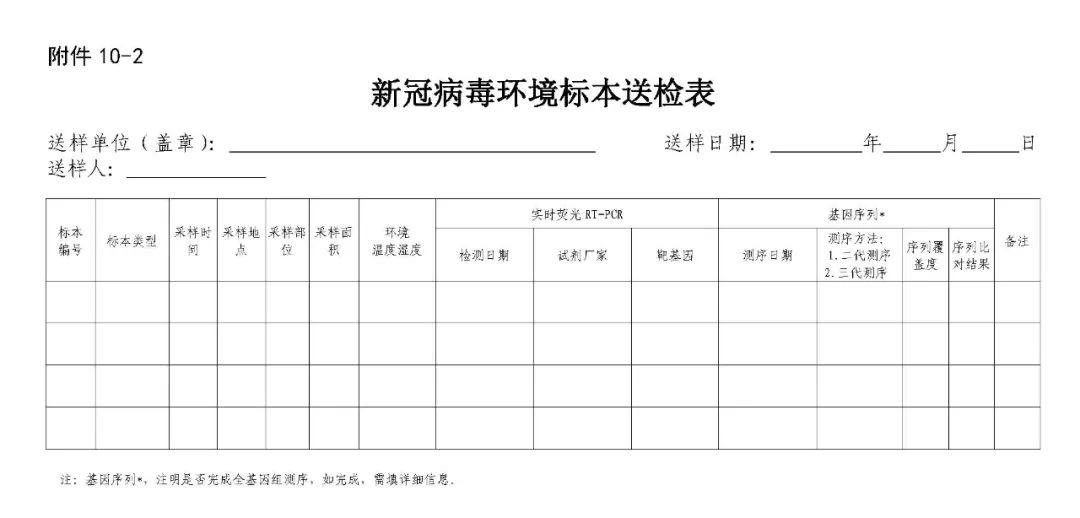
实验室检测技术人员应当具备实验室工作经历以及相关专业技术技能,接受过新冠病毒相关检验检测技能培训。检测机构应当按照所开展检测项目及标本量配备实验室检测人员,以保证及时、高效完成检测和结果报告。(1)核酸检测实验室。新冠核酸检测实验室按功能区布置位置的不同,可分为集中布置形式和分散布置形式。开展新冠病毒核酸检测的实验室应当设置以下区域:试剂储存和准备区、标本制备区、扩增和产物分析区。根据所采用仪器的实际情况,标本制备区、扩增和产物分析区可进行合并。集中布置形式的实验室设置应遵循“各区独立,单向流动(注意风向,压力梯度走向),因地制宜,方便工作”的原则。各区的功能如下: ①试剂储存和准备区:用于分装、储存试剂、制备扩增反应混合液,以及储存和准备实验耗材。该区应配备冰箱或冰柜、离心机、试验台、涡旋振荡器、微量加样器等。为防止污染,该区宜保持正压状态。 ②标本制备区:标本转运桶的开启、标本灭活(必要时)、核酸提取及模板加入至扩增反应管等。该区应配备冰箱或冰柜、生物安全柜、离心机、试验台、微量加样器,可根据实际工作需要选配自动化核酸提取仪等。标本转运桶的开启、分装应在生物安全柜内完成。为防止污染,该区宜保持负压状态。为操作方便,标本的分装以及核酸提取也可以在独立的生物安全二级(BSL-2)实验室进行,提取的核酸可以转运至该区加至扩增反应液中。 ③核酸扩增和产物分析区:进行核酸扩增反应和产物分析。该区应配备实时荧光定量PCR仪。为防止扩增产物污染环境,该区宜保持负压状态,压力等于或低于标本制备区。 实验室应当制定标准操作程序(SOP),并严格按照SOP进行操作。接到标本后,应当在生物安全柜内对标本进行清点核对,并依据SOP进行试剂准备、标本前处理、核酸提取、核酸扩增、结果分析及报告。实验室应当建立可疑标本复检的流程。①试剂准备。应当选择国家药品监督管理部门批准的试剂,建议选择磁珠法、膜吸附法等进行核酸提取,建议根据核酸提取试剂及扩增体系的要求选择配套的标本采样管,不建议免提取核酸直接进行核酸扩增反应。②标本处理。使用含胍盐等灭活型采样液的标本无需进行灭活处理,可直接进行核酸提取,而使用非灭活型采样液的标本,按照核酸提取试剂盒的说明,取适量标本加至核酸 提取裂解液中充分混匀作用一定的时间则可以有效灭活病毒。不推荐采用56℃孵育30分钟的处理方式灭活病毒,该条件不能保障充分灭活病毒。污水样本处理可参考《农贸(集贸)市场新型冠状病毒环境监测技术规范》(WS/T776—2021)推荐的方法。③核酸提取。将灭活后的标本取出,在生物安全柜内打开标本采集管加样。或按照核酸提取试剂盒的说明,将标本与裂解液作用足够时间后继续核酸提取步骤,核酸提取完成后立即封盖。取适量核酸加至PCR扩增反应体系中。④核酸扩增。将扩增体系放入荧光定量PCR仪,按照试剂盒说明书设置扩增程序,启动扩增程序。扩增完成后反应管不可开盖,直接放于垃圾袋中,封好袋口,不可高压,按 一般医疗废物转移出实验室处理。本指南中的核酸检测方法主要针对新冠病毒基因组中开放读码框1ab(open reading frame 1ab,ORF1ab)和核壳蛋白(nucleocapsid protein,N)。正向引物(F):CCCTGTGGGTTTTACACTTAA反向引物(R):ACGATTGTGCATCAGCTGA5'-FAM-CCGTCTGCGGTATGTGGAAAGGTTATGG-BHQ1-3'正向引物(F):GGGGAACTTCTCCTGCTAGAAT反向引物(R):CAGACATTTTGCTCTCAAGCTG5'-FAM-TTGCTGCTGCTTGACAGATT-TAMRA-3'阳性:Ct值小于等于检出限,且有S形扩增曲线,可报告为阳性。灰区:Ct值位于灰区,建议重复实验,若重做Ct值仍处于灰区,但出现明显的S形扩增曲线,该样本判断为阳性,否则为阴性。注:如使用商品化试剂盒,则以厂家提供的说明书为准。条件一:同一份标本中新冠病毒2个靶标(ORF1ab、N)实时荧光RT-PCR检测结果均为阳性。如果出现单个靶标阳性的检测结果,则需要重新采样,重新检测。条件二:两种标本实时荧光RT-PCR同时出现单靶标阳性,或同种类型标本2次采样检测中均出现单个靶标阳性的检测结果,可判定为阳性。环境与生物材料核酸检测阳性要排除疫苗接种物残留污染的影响。核酸检测结果假阴性的可能原因包括:样本质量差;样本采集时间过早或过晚;样本保存、运输和处理不当;其他原因如病毒变异、PCR抑制等。⑦质控。由上级疾控部门对下级疾控实验室进行核酸检测质控考核,中国疾控中心每年至少开展一次对省级疾控机构实验室的质控考核,并同时提供全国新冠病毒实验室检测质控方案,省级针对地市级实验室的质控考核每年不少于2次。各检测机构应当加强核酸检测质量控制,选用扩增检测试剂盒指定的核酸提取试剂和扩增仪。性能验证。临床标本检测前,实验室应对核酸提取试剂、提取仪、扩增试剂、扩增仪等组成的检测系统进行必要的性能验证,性能指标包括但不限于精密度(至少要有重复性)和最低检测限。建议选用高灵敏的试剂(检测限≤500拷贝/ml)。室内质控。实验室可按照《国家卫生健康委办公厅关于医疗机构开展新型冠状病毒核酸检测有关要求的通知》(国卫办医函〔2020〕53号)要求规范开展室内质控。每批检测至少有1份弱阳性质控品(第三方质控品,通常为检出限的1.5-3 倍)、3份阴性质控品(生理盐水)。质控品随机放在临床标本中,参与从提取到扩增的全过程。大规模人群筛查时,一旦出现阳性结果,应对阳性标本采用另外一到两种更为灵敏的核酸检测试剂对原始标本进行复核检测,复核阳性方可报出。物品和环境样本的采集检测,还需在采样前及采样过程中至少设一个现场空白样本及一个运输空白样本,以进行过程中的质量控制。室间质评。实验室应常态化参加国家级或省级疾控机构组织的室间质评。对检测量大以及承担重点人群筛查等任务的实验室,可适当增加室间质评频率。不按要求参加室间质评的,或室间质评结果不合格的,应通报批评并上报国家卫健委,待室间质评通过后方可开展核酸检测。(1)测序标本选取原则。结合流调信息和病例传播链关系,优先选择以下标本开展测序:本土疫情中的首发或早期病例、与早期病例有流行病学关联的关键病例、感染来源不明的本土病例、境外输入病例、入境物品及相关环境阳性标本、疫苗接种后核酸检测阳性者标本等。测序结果应与本地近一个月的输入病例和本土病例序列进行比对。(2)测序要求。以省为单位确定开展新冠病毒全基因组测序的单位,包括省、市级疾控机构和科研机构。各省要建立本省输入、本土病例新冠病毒基因组数据库,应具备序列对比分析能力。建议首选膜吸附法(人工)提取核酸,以二代测序技术进行新冠全基因组测序。具备测序条件的省份要在接收标本24小时内开展测序工作,关键样本要求收到样 本后一周内提供测序结果报告,并在获得测序结果后4小时 内将基因序列原始数据(一般为fastq格式) 和测序样本送检单(见附件10-2)报送中国疾控中心。不具备测序条件的省份要在病例报告后48小时内将病例标本送达中国疾控中心,中国疾控中心在获得序列信息后24小时内向送样单位反馈分析结果,并报国家卫生健康委。(3)上送标本要求。如标本需上送至中国疾控中心进行测序,应同时平行采集2次,混入1管中,然后平均分装成 2份,一份由各省(市)及时开展病毒全基因组测序,另一 份应在24小时内启动送样程序,上送中国疾控中心。如果需要中国疾控中心进行病毒分离,应确保病毒采样液中不含有 灭活剂成分。血清抗体检测(胶体金、磁微粒化学发光、ELISA)用作新冠病毒核酸检测阴性病例的补充检测,在疑似病例诊断中与核酸检测协同使用。建议采集急性期(发病7天内)和恢复期(3-4周后)双份血清进行检测,也可根据临床需要 确定采集时间。抗体检测阳性者应排除新冠疫苗接种因素的影响。根据新冠病毒传播特性、致病性和临床资料等信息,该病毒按照第二类病原微生物进行管理,具体要求如下:新冠病毒培养、动物感染实验应当在生物安全三级及以上实验室开展;未经培养的感染性材料的操作应当在生物安全二级及以上实验室进行,同时采用 不低于生物安全三级实验室的个人防护;灭活材料的操作应当在生物安全二级及以上实验室进行;不涉及感染性材料的操作,可以在生物安全一级实验室进行。各省级卫生健康行政部门要根据疫情防控需要和实验室生物安全有关要求,及时研判提出新冠病毒实验室检测生物样本处置意见。对确需保存的,应当尽快指定具备保存条件的机构按照相对集中原则进行保存, 或送至国家级菌(毒)种保藏中心保藏;对无需保存的,由相关机构按照生物安全有关要求及时处理。参考《医疗机构新型冠状病毒核酸检测工作手册》(试行第二版)。

|