肿瘤对于大众而言已不陌生,而肿瘤的治疗方式大体可分为手术、放疗以及化疗三大类,根据具体病情或使用单一治疗方式或联合治疗。化疗分为靶向治疗与非靶向(传统化疗)治疗两大类。伴随诊断需要通过对样本进行基因测序等分析手段进行药物受体作用位点的确定, 目前常用样本类型为组织以及体液。对组织进行分子分析的技术称为组织活检,具体是指应诊断、治疗的需要,从患者 体内切取、钳取或穿刺取出病变组织,对其进行分子分析。
对肿瘤伴随诊断来说,肿瘤 组织活检是获取肿瘤 DNA 的金标准。对液体进行分析的技术称为液体活检,具体是指 通过对患者的体液中的分析物(CTC、cfDNA、ctDNA 等)进行分子分析,以指导患者 的个性化治疗及预后,目前市面上的伴随诊断试剂盒大部分属于这一类型。
从临床应用上看,组织活检与液体活检各有优劣。虽然目前基于液体活检的肿瘤伴 随诊断近年来处于蓬勃发展之中,但并非意味着其已经能取代组织活检技术,两者合作 互补或许能大大提高诊断效率,减少过度治疗。随着液体活检技术不断发展,未来基于液体活检的肿瘤伴随诊断或将进一步替代组织活检技术,成为伴随诊断检测的主力军。

传统化疗药物是以细胞分裂周期为核心, DNA、RNA和蛋白质的合成为主要线索发挥治疗作用的。作用的时点是细胞分裂的周期,简而言之传统化疗就是针对一切细胞分裂起作用,并不区分正常细胞和肿瘤细胞。只是肿瘤细胞分裂速度快作用大、而正常人体细胞分裂速度慢而影响相对小。
肿瘤靶向药则是根据细胞信号传导的机理,以细胞信号传导过程中的特定蛋白质作为靶点的药物,通过和特定的蛋白质结合,阻止细胞信号的传导。靶点蛋白是研究中发现的肿瘤细胞有但正常细胞没有,或肿瘤细胞多但正常细胞极少的,作用于细胞信号传导通路关键节点的蛋白质,因此可以产生特定的抗肿瘤作用,而对正常细胞影响较传统化疗小。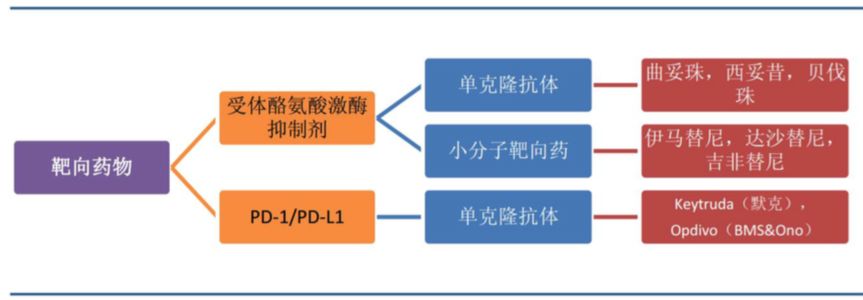
但是以特定蛋白质作为靶点的单抗或者替尼类靶向药,一旦靶标蛋白的基因突变,就会导致靶蛋白结构改变,出现药物“脱靶”或疗效不佳的情况,所以在使用靶向治疗之前,须通过基因检测的手段测试药物的有效性,使用的基因检测方法包括 PCR、 FISH 和测序等。

因此,靶向药的治疗前提之一便是针对特定靶点的基因检测,所以说肿瘤伴随诊断是随着靶向治疗技术的发展应运而生的行业,甚至可以说靶向药的发展直接决定肿瘤伴随诊断的发展一点不为过。 肿瘤伴随诊断专有技术
一、肿瘤个性化用药指导基因检测技术
肿瘤个体化用药指导基因检测技术主要通过检测肿瘤患者的基因变异情况,为临床 医生诊疗及用药提供依据。采用二代高通量测序技术、Sanger 测序技术、MALDITOF-MS(基质辅助激光解吸电离飞行时间质谱)等成熟的基因检测技术,利用前沿的生物信息分析技术,建立了全球权威的用药基因变异解读数据库,根据基因变异和数据库 信息,为临床医生提供全方位、有效的诊疗依据。
二、Oseq™-ctDNA 无创肿瘤个体化诊疗基因检测技术
Oseq™-ctDNA 技术仅需抽取少量外周血进行肿瘤基因检测,解决了无法通过手术 或穿刺取得癌症组织的患者的诊疗难题,采用新一代目标区域捕获结合高通量测序、内 部数据库与信息分析技术,一次性检测与癌症发生和药物靶点相关基因的外显子和部分 内含子区域。针对所有实体瘤患者,详细了解肿瘤患者特有基因变异情况,为晚期肿瘤 患者提供无创的肿瘤基因检测,及时准确地监测患者基因变异,提供精准的药物方案, 根据患者基因的个体差异性协助医生选择合适药物和制定更完善的治疗方案,最大程度 地满足患者对治疗的个性化需求。
肿瘤伴随诊断行业受益于靶向药的快速成长而保持高速发展靶向药行业的增长主要取决于肿瘤患者的发病率提升、靶向药的发展以及靶向药价格下降三大因素。(1)从全球范围来看,根据世界卫生组织《2015全球癌症统计》数据披露,2012年全球恶性肿瘤新发病例约1410万,比2008年的数据增加约11%,其中男性新增7,427,100人,女性新增6,663,000人;其中,新发恶性肿瘤最常见的依次为肺癌(180万,13%)、乳腺癌(170万,11.9%)和结直肠癌(140万,9.7%)。随全球人口增长与老龄化的加剧,恶性肿瘤已成为世界范围内的主要死因。预计到2025年前,全球每年新增癌症病例数将高达1930万例。表五:2012年全球男/女性主要新增癌症种类及主要死亡种类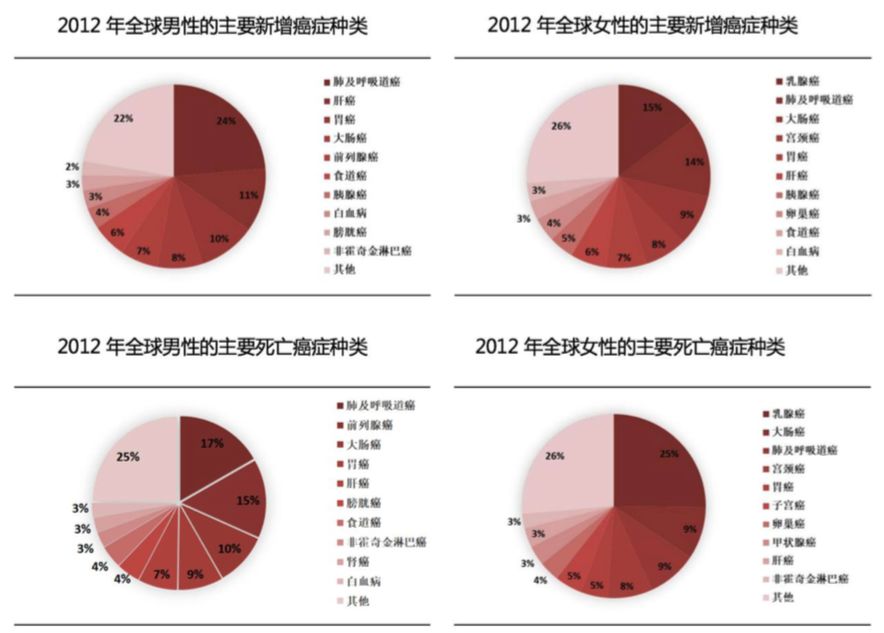
(2)从中国地区来看,根据2017年中国肿瘤登记年报数据显示与2012年相比,癌症新发人数继续上升,从358万增加到368万,增幅3%;全国每天约1万人确诊癌症,每分钟约7人确诊患癌。自40岁开始癌症发病率快速上升,至80岁达到高峰,中国城市居民0-85岁的累计癌症发生风险高达36%。其中,肺癌为发病率、死亡率双率第一,已与发达国家水平相当;甲状腺癌发病率上升趋势快,需格外引起重视。死亡率排前的癌症主要是肺癌和消化系统癌症。
当前,城市地区男性最普遍的5种癌症依次为:肺和支气管癌症、胃癌、肝癌、食管癌、结直肠癌,这些占到所有癌症病例的三分之二;女性中最普遍的5种癌症依次为:乳腺癌、肺和支气管癌、结直肠癌、胃癌及甲状腺癌,甲状腺癌快速上升,乳腺癌占所有女性癌症的15%。
全球范围内靶向药新药研发迅猛、部分已上市靶向药进入医师用药指南一线治疗方案以及靶向药适应症的逐步扩大。 (1)全球范围内靶向药新药研发迅猛,以美国为例,过去十年间FDA 新批的肿瘤药物中,靶向药物数量显著超越传统化疗药物。表七:2005-2014 年美国 FDA 新批肿瘤治疗药物
目前处于临床试验阶段的,替尼类药物至少超过50种,数量远远超过目前已经上市的品种。中国:目前只有恒瑞医药和浙江贝达分别具有一个1.1类的替尼药物,阿帕替尼和埃克替尼。但是目前正在进行临床实验的国产替尼药物数量明显增多。
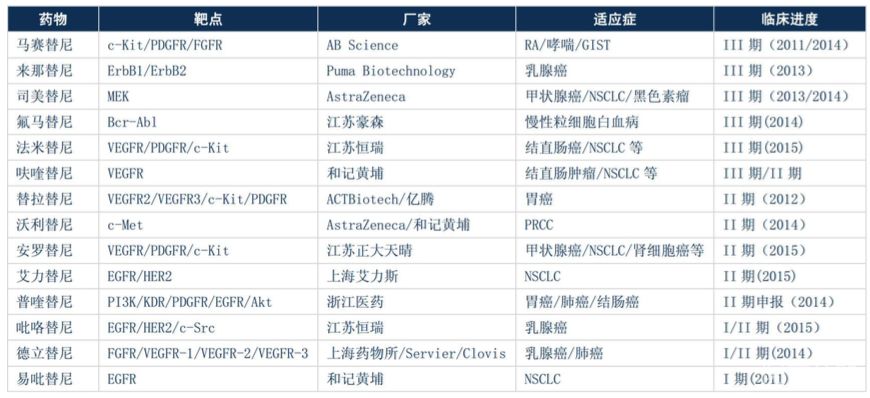
(2)部分已上市靶向药进入医师用药指南一线治疗方案以及靶向药适应症的逐步扩大
埃克替尼已获批用于基因敏感突变的局部、晚期或转移性非小细胞肺癌患者的一线治疗。厄洛替尼FDA已批准用于一线治疗转移性非小细胞肺癌。吉非替尼适用于单药继续治疗铂类和多西他赛化疗失败的局部晚期或转移性非小细胞肺癌,现已用于肺癌一线治疗。曲妥珠单抗还被批准单独应用于已接受一次或多次化疗疗程的 HER2+ 乳腺癌患者的治疗,以及与紫杉醇联合作为 HER2+ 乳腺癌的一线治疗。2018年1月勃林格殷格翰公司宣布 FDA扩大阿法替尼一线适应症范围。中国医师用药指南靶向药一线治疗方案滞后于美国,存在更大临床使用提升空间。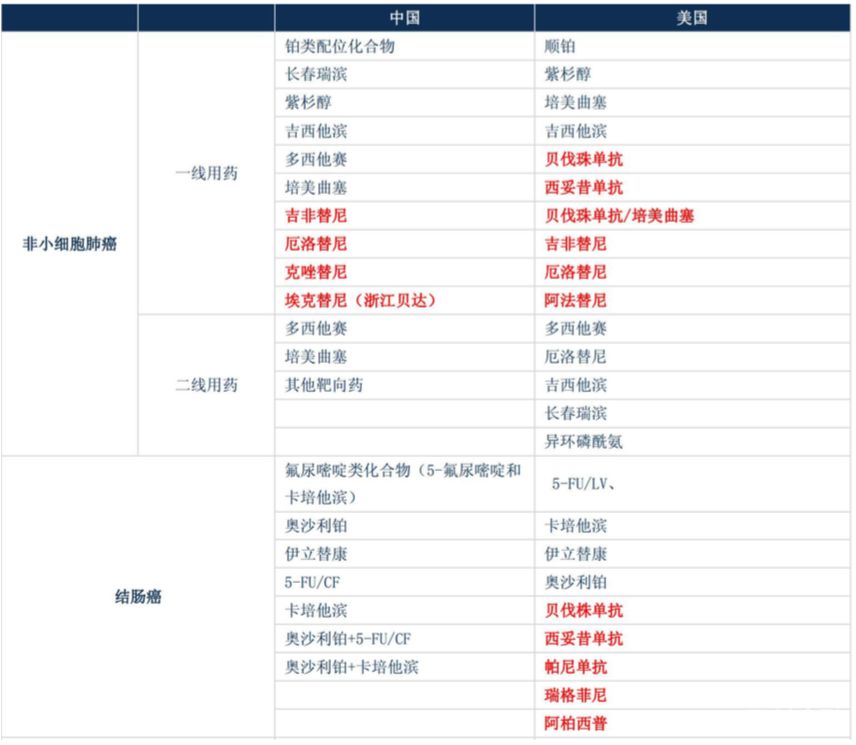
中国地区尚存在大量未引进已上市靶向药,存在进一步靶向药提升的市场空间。国内创新药目前处于加速上市期:奥希替尼进入CFDA 快速审批通道,从受理(2016年9 月)到上市申请批准(2017年3月),仅用了7个月;帕唑帕尼由葛兰素史克(GSK)研发,于2017年2月21日获中国食品药品监督管理总局(CFDA)批准上市。国务院总理李克强2018年3月20日在回答中外记者提问时提到“患者急需的抗癌药品,我们要较大幅度地降低进口税率,对抗癌药品力争降到零税率。” 抗癌药物零关税,以及前不久推出的药物审批方面的一些改革措施,都是为了推进创新药物在中国的上市速度。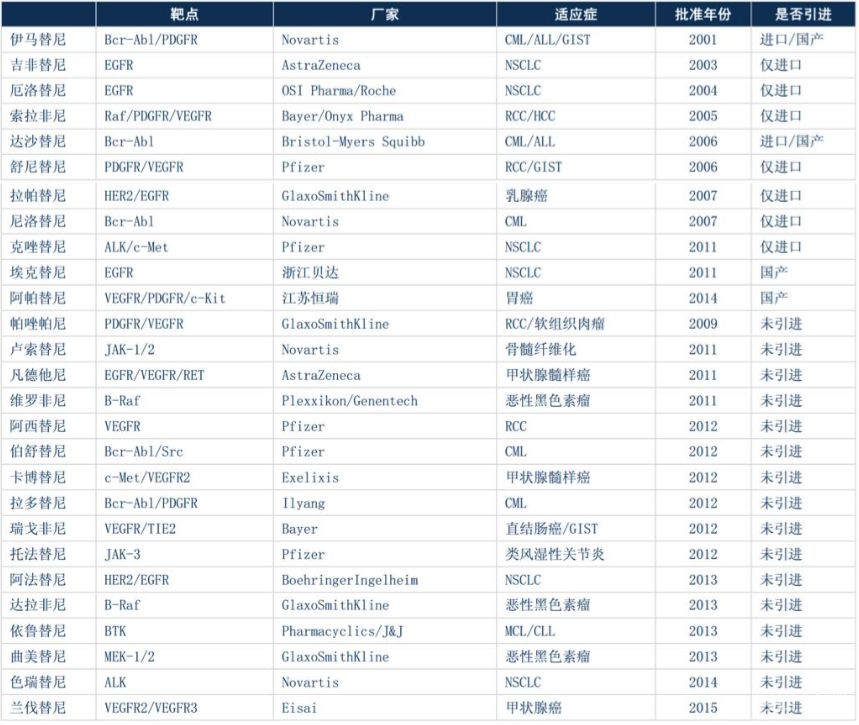
3、靶向药迎来降价潮、部分靶向药进入中国医保支付范畴靶向药大部分是专利药,价格昂贵,但部分品种随着印度仿制药的冲击、竞争新药的上市以及中国医保价格谈判,迎来降价潮。例如:吉非替尼进入医保乙类,0.25g 规格的药品最小制剂单位价格在170元左右,较之前价格降幅在40-50%;厄洛替尼进入医保乙类后,0.15g规格的药品最小制剂单位价格在195元,降幅在50%以上;泰立沙在中国属于医保乙类用药,进入医保乙类后,0.25g规格的药品最小制剂单位价格从原来的121元降至70元,降幅在42%,埃克替尼进入医保乙类后,其0.125g规格的药物最小制剂单位价格是67元,降幅在50%左右。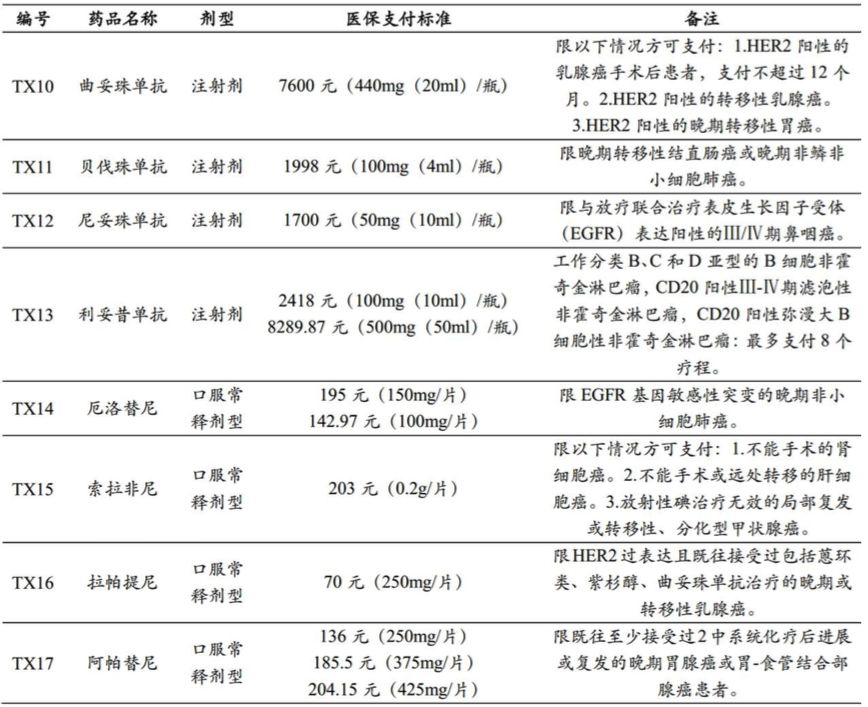
2017年全球伴随诊断市场规模约为52亿美元,其中美国作为最大的伴随诊断市场,规模约为16亿美元,国内市场规模约2.22亿美元左右,诊断市场容量保持了20%以上的CAGR。
总体而言,肿瘤伴随诊断随着靶向药的快速发展而发展,靶向药未来持续成长体现在肿瘤发病率的居高不下、靶向药研发快速增长、适应症在逐步扩大、用药指南逐步提升至一线用药方案、靶向药的降价以及医保的覆盖,使用人群逐步增大,肿瘤伴随诊断产品使用率存在长期、持续提升空间。