|
患者女性,31岁,未婚未育。主诉:四肢浮肿7年,双下肢肿痛半月余,加重1周。
7年前出现四肢浮肿,就诊于本市某三甲医院,诊断为“系统性红斑狼疮、狼疮肾炎Ⅳ型”,予以口服甲强龙40mg、羟氯喹0.2 qd、吗替麦考酚酯0.75 bid常规治疗。后因考虑生育需求,更换为环孢素治疗,并口服糖皮质激素2片。从2020年起使用“泰爱”治疗至2022年12月。 此次半月余前,患者再次出现双下肢肿痛,左下肢明显,伴疼痛发红,皮温升高,有光过敏,就诊我院风湿科门诊,拟“下肢肿胀”收入院。既往体健,无特殊。体格检查:体温 36.2℃、脉搏 94次/分、呼吸 20次/分、血压 138/96mmHg,双下肢肿胀,皮温高,余正常。血红蛋白 89.00↓g/L、红细胞计数 3.09↓* 1012/L、中性粒细胞占比 82.20↑%。血清磷 1.76↑mmol/L、葡萄糖 7.51↑mmol/L、尿素 10.61↑mmol/L、钙 2.03↓mmol/L、甘油三脂 2.99↑mmol/L、载脂蛋白B 1.18↑g/L、尿酸 568↑umol/L、肌酐 155↑umol/L、胆固醇 5.60↑mmol/L、乳酸脱氢酶 395↑U/L、谷氨酰基转移酶 60↑U/L、肌酸激酶 37↓U/L、总蛋白 64.7↓g/L、白蛋白 30.1↓g/L、白/球 0.87↓。D-二聚体 4.4↑ug/mL、纤维蛋白原 4.17↑g/L、纤维蛋白降解产物 13.5↑ug/mL。IL-6 13.00↑pg/mL、TNFa 51.4pg/ml。直接Coombs试验(总抗体)阳性(+) 、直接Coombs试验抗人IgG阳性(+) 、直接Coombs试验抗人C3d阳性(+)。IgE 360.000↑IU/ml、CRP 13.700↑mg/L、IgM <0.182↓g/L、补体C3 0.740↓g/L。尿潜血2+、尿蛋白1+、24小时尿总蛋白定量检测 826↑mg/24h。CD3+ 87.2↑%、CD3+CD4+ 28.6%、CD3+CD8+ 57.1↑%、CD3+CD4+/CD3+CD8+ 0.50↓、CD3-CD19+ 3.3↓%、CD3-CD16+CD56+ 10.3%。血沉 108↑mm/h、25-羟基维生素D 5.45↓ng/ml、促甲状腺激素 7.594↑mIU/L、硫酸去氢表雄酮 <15.0↓μg/dl、超敏肌钙蛋白-T 28.60↑pg/mL、降钙素原 0.1590↑ng/mL。抗双链DNA(抗dsDNA)抗体中阳性 (++)、抗组蛋白抗体(AHA)弱阳性 (+)、抗核小体抗体(AnuA)强阳性 (+++),抗SSA、抗SSB、抗Scl-70、抗Jo-1、抗CENP-B、抗Sm、抗nRNP/Sm、抗Ro-52、抗核糖体P蛋白抗体均阴性。pANCA (+) 、抗髓过氧化物酶MPO (+)、抗环瓜氨酸肽抗体 1.0RU/ml。抗心磷脂抗体IgA型/IgG型/IgM型、抗β2糖蛋白1抗体IgA型/IgG型/IgM型定量检测均阴性。核型为均质型,滴度1:2560,采用AESKU的抗核抗体检测试剂盒(间接免疫荧光法),2倍稀释体系,起始稀释度1:80。
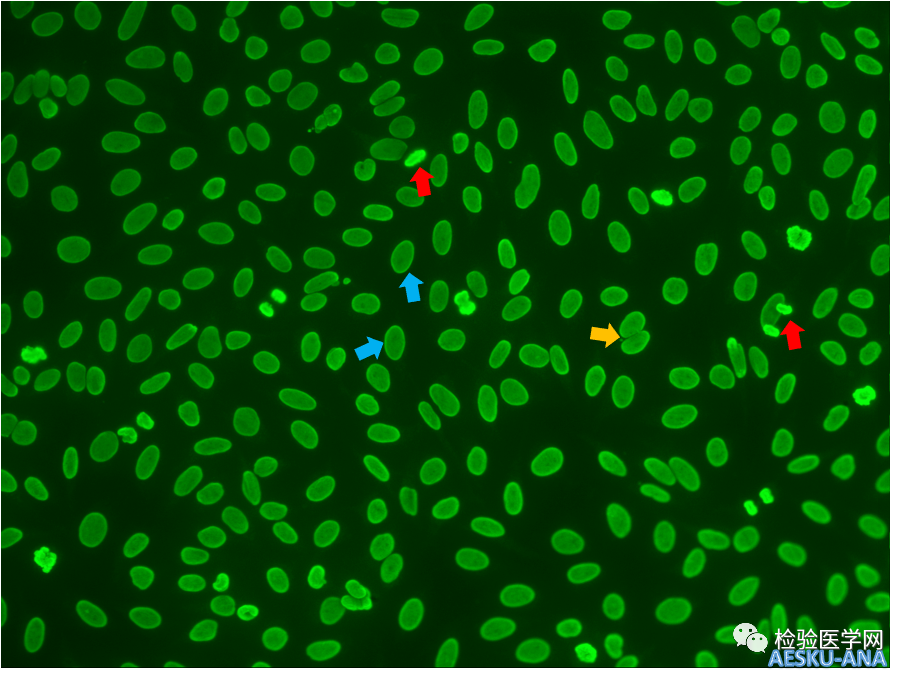
图1 ANA-IIF(1:80,AESKU,显微镜倍数200×) HEp-2细胞作为基质,蓝色箭头表示间期细胞核连续的光滑核膜增强荧光,橙色箭头表示相邻细胞核接触部分无增强荧光,红色箭头表示分裂中晚期浓缩染色体在强荧光下呈现“返空”现象。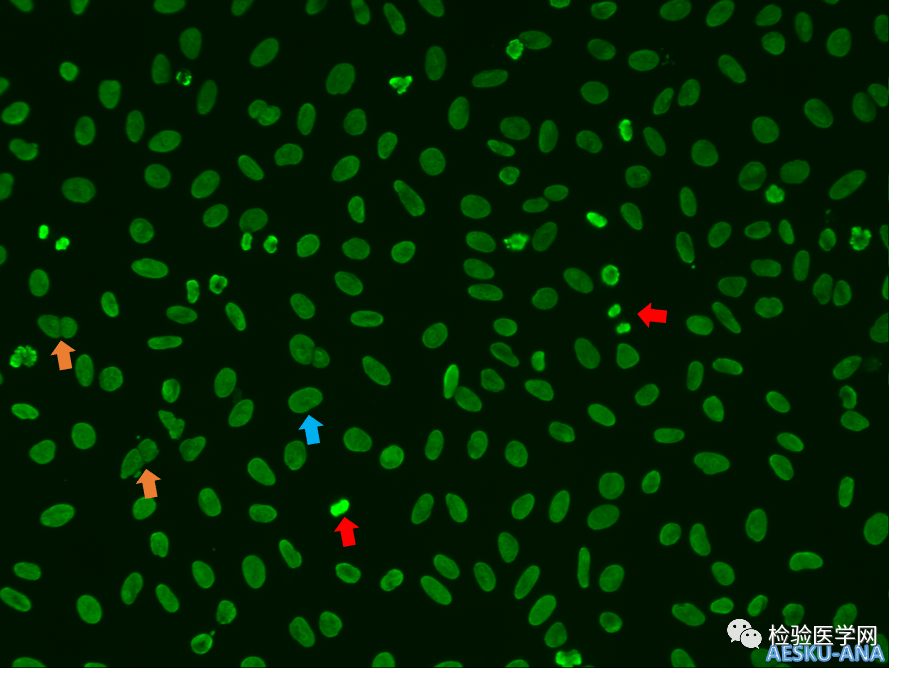
图2 ANA-IIF(1:2560,AESKU,显微镜倍数200×) HEp-2细胞作为基质,蓝色箭头提示间期细胞核膜周围增强荧光减弱,红色箭头提示分裂期中晚期浓缩染色体呈现均一、玻璃样增强荧光,橙色箭头提示相邻细胞核膜间未见增强荧光。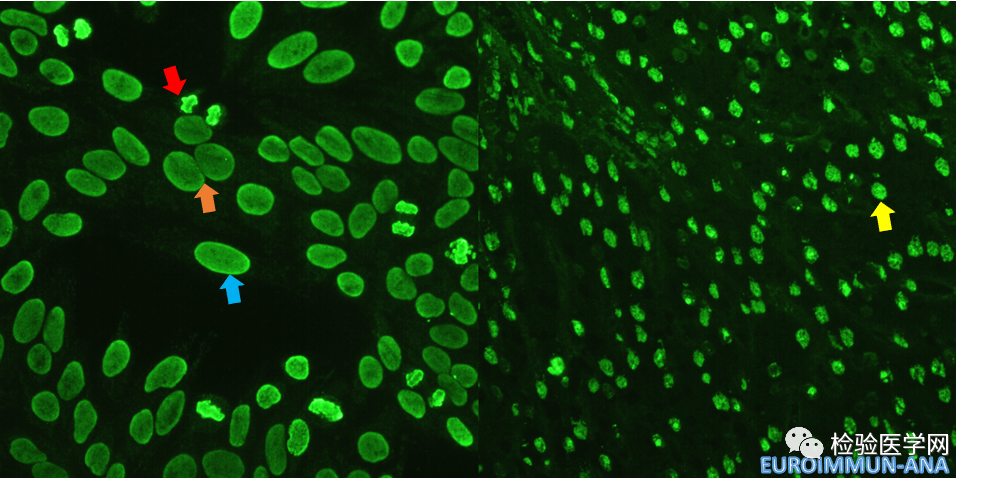
图3 ANA-IIF (1:100,EUROIMMUN,显微镜倍数400×)左侧为HEp-2细胞基质片,右侧为猴肝组织片,蓝色箭头提示间期细胞核周围的连续光滑增强荧光,红色箭头提示分裂期浓缩染色体的“返空”现象,橙色箭头提示相邻细胞核膜无增强荧光。黄色箭头提示猴肝细胞核阳性。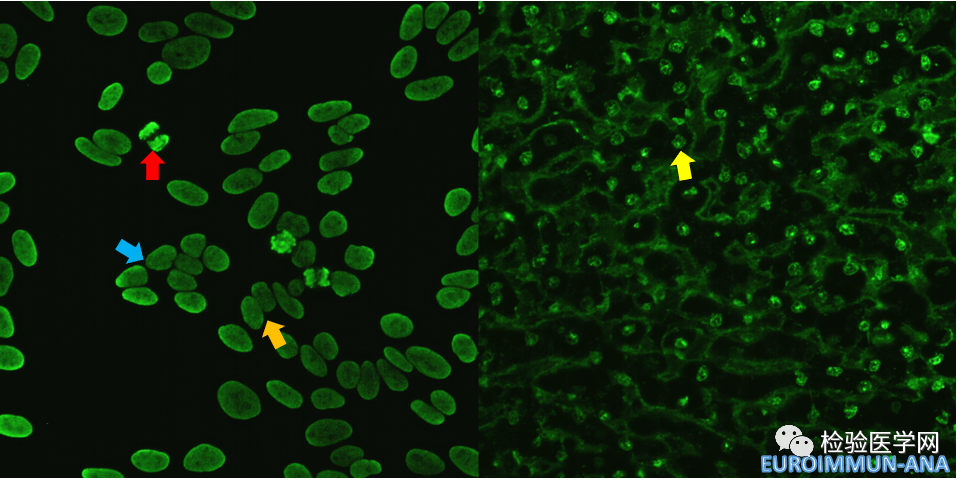
图4 ANA-IIF (1:1000,EURIMMUN,显微镜倍数400×) 左侧为HEp-2细胞基质片,右侧为猴肝组织片,蓝色箭头提示间期细胞核周连续光滑增强荧光减弱,红色箭头提示分裂期浓缩染色体的“返空”现象消失,浓缩染色体均匀增强荧光,橙色箭头提示相邻细胞核膜无增强荧光。黄色箭头提示猴肝细胞核阳性。
该样本进行ANA荧光检测首次阅片时(见图1),可见HEp-2细胞核(起始稀释度为1:80)在分裂间期呈现均质荧光,核周周围有连续的光滑核膜增强荧光,核仁阳性;在分裂中期和后期,浓缩染色体在强荧光下呈现“返空”现象,误读为阴性,因此初判ANA核型为光滑核膜型。由于光滑核膜型在临床工作中较为少见,因此经复核阅片,以及本实验室例行阅片会共同读片后发现:未见到相邻细胞核膜接触部分的增强荧光,光滑核膜型证据不足,该片荧光过强,可能干扰核型判读;此外,该患者抗核抗体谱中检出AHA、AnuA自身抗体阳性,抗dsDNA抗体阳性;经讨论,对该标本进行连续稀释检测,同时采用欧蒙的抗核抗体IgG检测试剂盒(间接免疫荧光法)进行平行检测。血清样本经过稀释后,AESKU试剂在1:2560稀释度(见图2)呈现弱阳性荧光,HEp-2基质细胞核在分裂间期,核周连续的光滑核膜荧光减弱甚至消失,分裂中晚期浓缩染色体呈均一、玻璃样的增强荧光,荧光淬灭导致的“中空”现象消失,呈现典型的核均质型荧光核型。在平行检测中,使用欧蒙试剂,在起始1:100稀释度(见图3)中HEp-2基质表现与AESKU试剂起始稀释度为1:80的荧光特点相似,但在猴肝组织片中,可见肝细胞核阳性,呈均一、有时为粗或细的块状荧光,荧光强度与HEp-2细胞基本一致。如若为光滑核膜型,则肝细胞核是呈现特征性的环状荧光。在1:1000稀释度(见图4)呈现中等强度荧光,分裂间期的HEp-2细胞核荧光减弱,分裂中晚期浓缩染色体荧光为均一玻璃样荧光,返空现象消失;当1:10000稀释度时荧光阴性,在3.2倍稀释体系中,报ANA滴度为1:3200。
1.系统性红斑狼疮、狼疮性肾炎IV型;2.下肢静脉血栓形成(左侧股浅静脉下段、腘、肌间静脉))。
针对系统性红斑狼疮,甲泼尼龙和生物制剂“利妥昔单抗”治疗,调节免疫。针对左侧股浅静脉下段、腘、肌间静脉血栓症,予以低分子肝素和华法林抗凝,并予莫西沙星抗感染,辅以其他对症治疗等。现患者下肢浮肿消退,疼痛缓解。复查下肢血管彩超,提示血栓部分再通,予办理出院,门诊复诊。
系统性红斑狼疮(SLE)是累及多系统,存在多种自身抗体的异质性、复杂的系统性自身免疫性疾病,多见于育龄期女性。
常见的自身抗体及发生率为:抗dsDNA抗体(60%~90%)、AHA(30%~70%)、AnuA(40%~70%)、抗Sm(10%~30%)、抗SSA(20%~60%)、抗SSB(10%~20%)、抗Ro-52(38%)、RIB(10%)、抗增殖性细胞核抗原(PCNA)(3%)等。
其中抗dsDNA是SLE患者最为突出的血清标记抗体,抗dsDNA滴度升高与疾病严重程度呈正相关;此外AnuA诊断特异性可达95%,与病情活动相关;抗Sm、PCNA、RIB也是SLE特异性抗体,但是阳性率低;AHA则常见于药物诱导的红斑狼疮。 本病例患者系统性红斑狼疮-狼疮肾炎(IV)诊断明确,合并下肢静脉血栓症,存在抗dsDNA、AHA、AnuA自身抗体,都是均质型相关靶抗原,ANA荧光结果为均质型,滴度1:2560,高滴度的均质型主要见于SLE患者。在某些情况下,均质型由于洗片过度或者抗DNA抗体与核周围的异染色体发生反应,而产生类似核周连续环状增强荧光,易和光滑核模型混淆,但其增强荧光较光滑核膜型宽,且相邻细胞核接触部分没有荧光增强,而光滑核膜型相邻细胞核膜接触部分则有荧光增强。另外鉴别要点:在分裂期各期,均质型浓缩染色体阳性,而光滑核膜型阴性。此外,光滑核膜型相关的靶抗原不同于均质型,主要为核纤层蛋白A、核纤层蛋白B、核纤层蛋白C和核纤层相关蛋白。
首次阅片误判ANA核型为光滑核膜型还有另外一个因素,就是该荧光片在起始稀释度1:80呈强荧光强度,分裂中期和后期浓缩染色体在强荧光下导致中间荧光淬灭而呈现“返空”现象,误读阴性。
针对强荧光片而出现的中空或者反阴现象,这就需要检验人员对样本稀释后再测,再判读核型。对不典型或者复合核型,仅单一的HEp-2基质片无法准确判读时,可以采用HEp-2基质片+猴肝组织片组合试剂进行平行检测,辅助判断。这是因为不同核型在猴肝组织中有不同的表现,这有助于HEp-2基质细胞核核型的判读和鉴别。
综上,作者认为,抗核抗体核型的报告应结合抗核抗体谱结果、患者病史及其他辅助检查综合判断;此外,不同试剂的平行检测也提供了非常重要的证据。在检验工作中,不典型的、复合的核型是常见的,这就需要检验人员经过专业培训,熟练掌握各核型判读的特征,再结合其他临床表征综合判读,从而为临床诊疗提供更确切的诊疗依据。[1] 郑冰,吕良敬,李敏,等.抗核抗体荧光核型图谱及病例判读[M].上海:上海科学技术出版社,2021:362.[2] Shoenfeld, Y, Meroni, PL, Gershwin ME, et al. Autoantibodies[M]. 3rd ed. Amsterdam: Elsevier, 2014.[3] Sui M, Lin Q, Xu Z, et al. Simultaneous positivity for anti-DNA, anti-nucleosome and anti-histone antibodies is a marker for more severe lupus nephritis[J]. Journal of clinical immunology, 2013, 33(2): 378-387.
|